上海泽威信息科技有限公司
地址:上海市松江区东宝路19号东宝大厦602室
电话:86 21-3126 1348
电话:86 21-5771 2250
传真:86 21-5771 2250
电邮:cvtest@126.com
QQ:870335905
QQ:578020381
Wechat:wx578020381

美国FDA在4月3日在其官网上专门发布针对中国生产的非NIOSH认证的口罩如何申请EUA紧急授权的文件。美国FDA曾经不认可中国标准的KN95口罩,这一新发布的文件,标志着按照中国标准生产的KN95口罩得到FDA认可。
在目前疫情爆发期间企业可以申请EUA紧急授权,对于想长久经营的企业建议同时申请NIOSH认证。
办理EUA需受到FDA的监管,企业要承诺符合以下条件,以便随时接受FDA调查。
A. 厂商必须提供EUA授权的型号的用途,使用方法,和其他说明(如适合性测试等)。
B. 厂商要提供一封英文信函分发给各类终端用户(比如说医院),这封信函必须包括授权口罩的制造商、型号、预期用途、制造商网页等。
C. 厂商必须通知进口商本EUA的条款和条件,并确保接收授权口罩的终用户设施(如各医院等)收到条件B要求的信息。
D. 授权厂商要建立一个报告不良事件的程序,并将这些报告发送给FDA.
E. 所有描述性印刷材料应与COVID-19爆发期间使用的适用CDC建议以及本EUA中规定的术语一致。(也就是说不能宣传与本产品实质情况不符合的防护能力)
F. 任何与在美国使用授权口罩有关的描述性印刷品均不得表达或暗示该产品对预防COVID-19是安全或有效的。
G. 授权口罩的厂商将确保与本EUA相关的任何记录得到保存,直到FDA另行通知。根据要求,这些记录将提供给FDA检查。
EUA申请的范围是中国生产的一次性防护口罩,立体型。医用平面口罩不在范围内。
未经任何NIOSH认证的中国制造防护口罩只要满足以下三个条件之一即可向FDA申请紧急批准(EUA)。
1. 工厂生产的其他型号通过了NIOSH认证
2. 满足其他国家的市场准入并获得FDA验证
3. 有资质的第三方检测报告能够证明产品满足相关标准,并可以提供证明给FDA验证(根据中国的相关标准进行设计和验证的产品)
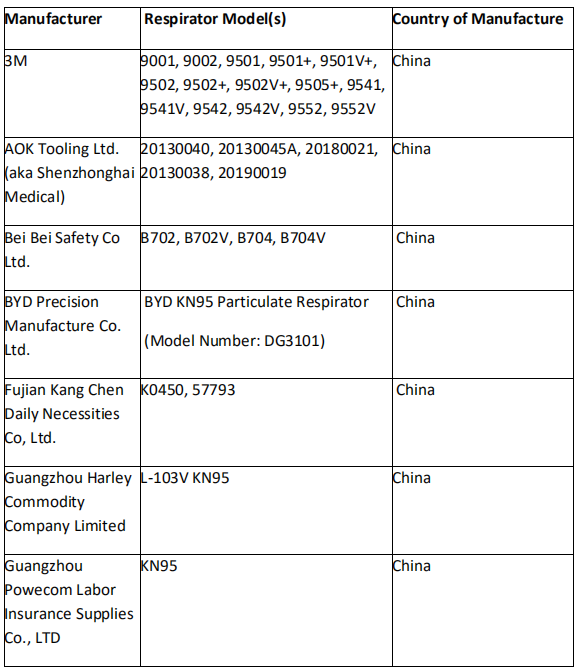
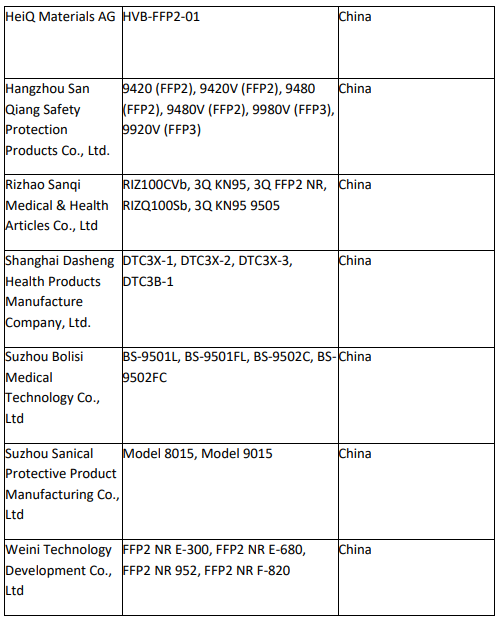
目前依据2020.5.7号颁发的新的EUA授权法案,已经获得EUA授权的企业很多已经被取消授权,只剩下如下企业: