上海泽威信息科技有限公司
地址:上海市松江区东宝路19号东宝大厦602室
电话:86 21-3126 1348
电话:86 21-5771 2250
传真:86 21-5771 2250
电邮:cvtest@126.com
QQ:870335905
QQ:578020381
Wechat:wx578020381

最近我们注意到,5 个样品的细菌过滤效率(BFE)、压差(Delta P)和颗粒过滤效率(PFE)可能不再适合提交FDA 510k 申请。在过去,许多制造商至少测试5 个样品的Delta P, BFE,和PFE,历史上这个数量已经成功地通过FDA 510k 批准。但根据最近从FDA收到的信息,FDA 正在强化标准ASTM F 2100 中所述的抽样要求,如下所示:
7. 抽样
7.1 需要对生产口罩的材料执行测试
7.2 为确保医用口罩符合特定性能等级的所有测试要求,应使用4%的可接受质量限值。
7.3 可接受的抽样计划参考,见ANSI/ASQC Z1.4 和ISO2859-1。
8. 测试的数量
8.1 每次测试应评估足够数量的医用口罩,以达到既定的可接受质量限制或置信度。
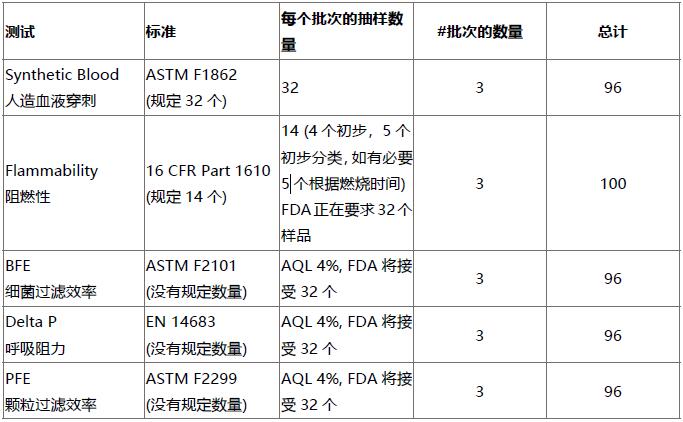
除了ASTM F2100 规范,FDA 还要求制造商测试最多3 个非连续批次,以证明每个批次的性能,或提供没有这样做的原因证明。对于FDA510k 的提交,我们建议您采取最保守的方式,以防止提交过程中的任何延误。下表是我们根据最近趋势提出的建议: